Vật liệu lưu trữ Hyđrua kim loại
Nghiên cứu vật liệu lưu trữ hydrua kim loại của Văn phòng Công nghệ Pin Nhiên liệu và Hydro (HFTO) tập trung vào việc cải thiện khả năng thể tích và trọng lượng, động học hấp phụ/giải hấp hydro, vòng đời và nhiệt động lực học phản ứng của các vật liệu tiềm năng.
Trung tâm Xuất sắc về Kỹ thuật Lưu trữ Hydro đã phát triển biểu đồ chiếu hệ thống hiển thị hệ thống natri alanat (SAH) được mô hình hóa và cách so sánh hệ thống này với tất cả các mục tiêu năm 2020 của DOE.
Tổng quan về kỹ thuật
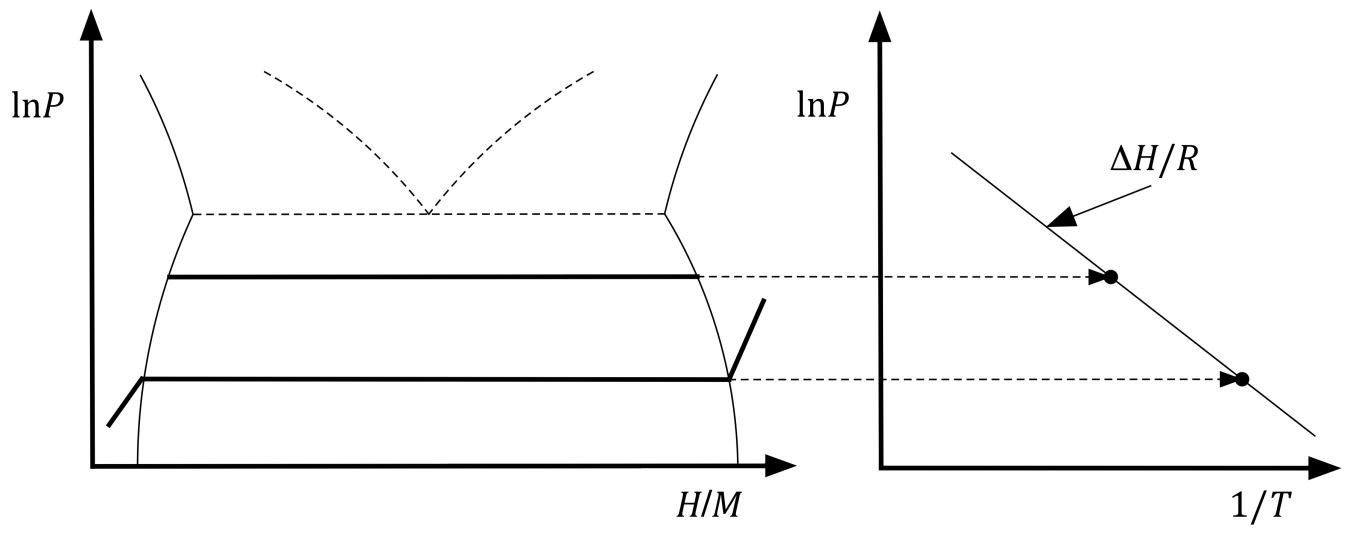
Hình 1. Đường đẳng nhiệt thành phần áp suất ở bên trái minh họa cách sử dụng áp suất cân bằng ở một nhiệt độ nhất định để xác định độ dốc của đường van't Hoff được hiển thị ở bên phải.
Hyđrua kim loại (MHx) là loại vật liệu lưu trữ hydro phù hợp nhất về mặt công nghệ vì chúng có thể được sử dụng trong nhiều ứng dụng bao gồm điều chế neutron,1 chu trình điện hóa,2 lưu trữ nhiệt,3 bơm nhiệt,4 và tinh chế/tách.5 Trong khi nhiều loại khác kim loại kiềm hoặc sp cũng tạo thành hydrua muối hoặc cộng hóa trị, việc nhận biết rằng hydrua kim loại chuyển tiếp, đặc biệt, trên thực tế là các hợp chất riêng biệt được phân biệt với dung dịch rắn của hydro là nhờ các tính toán cấu trúc dải của Switendick.6 Tuy nhiên, thuộc tính liên quan nơi các giải pháp ứng dụng được tìm kiếm là vùng dung dịch rắn của sơ đồ pha, giữa các pha kim loại và hydrua như trong Hình 1.
Nhiệt động lực học của quá trình hấp phụ/giải hấp hydro chi phối phạm vi áp dụng và nhiệt độ của chúng. Entanpy và entropy trên vùng áp suất không đổi của biểu đồ pha có thể được mô tả bằng cách áp dụng năng lượng tự do Gibbs đẳng nhiệt vào phương trình van't Hoff để thu được dạng tuyến tính:
ln(P) = ΔH/RT - ΔS/R
Do đó, nhiệt động lực học trên vùng dung dịch rắn được trình bày dưới dạng sơ đồ có thể liên quan đến ln(P). Entanpy ΔH là âm đối với loại này, phản ánh sự giải phóng nhiệt thu năng của hydro cho phản ứng.
Việc phân tích đặc tính nhiệt động đặc biệt quan trọng đối với các yêu cầu áp suất cân bằng dành riêng cho ứng dụng. Mặc dù giá trị cân bằng 1 bar thường được dùng để xác định giá trị hoặc phạm vi ΔH thích hợp, nhưng pin nhiên liệu màng điện phân polyme (PEM) có thể yêu cầu áp suất lớn hơn 5 bar. Do đó, phương trình van't Hoff có thể được sử dụng để đánh giá bước đầu khả năng tồn tại của hydrua đối với một ứng dụng cụ thể trong phạm vi nhiệt độ và áp suất vận hành.
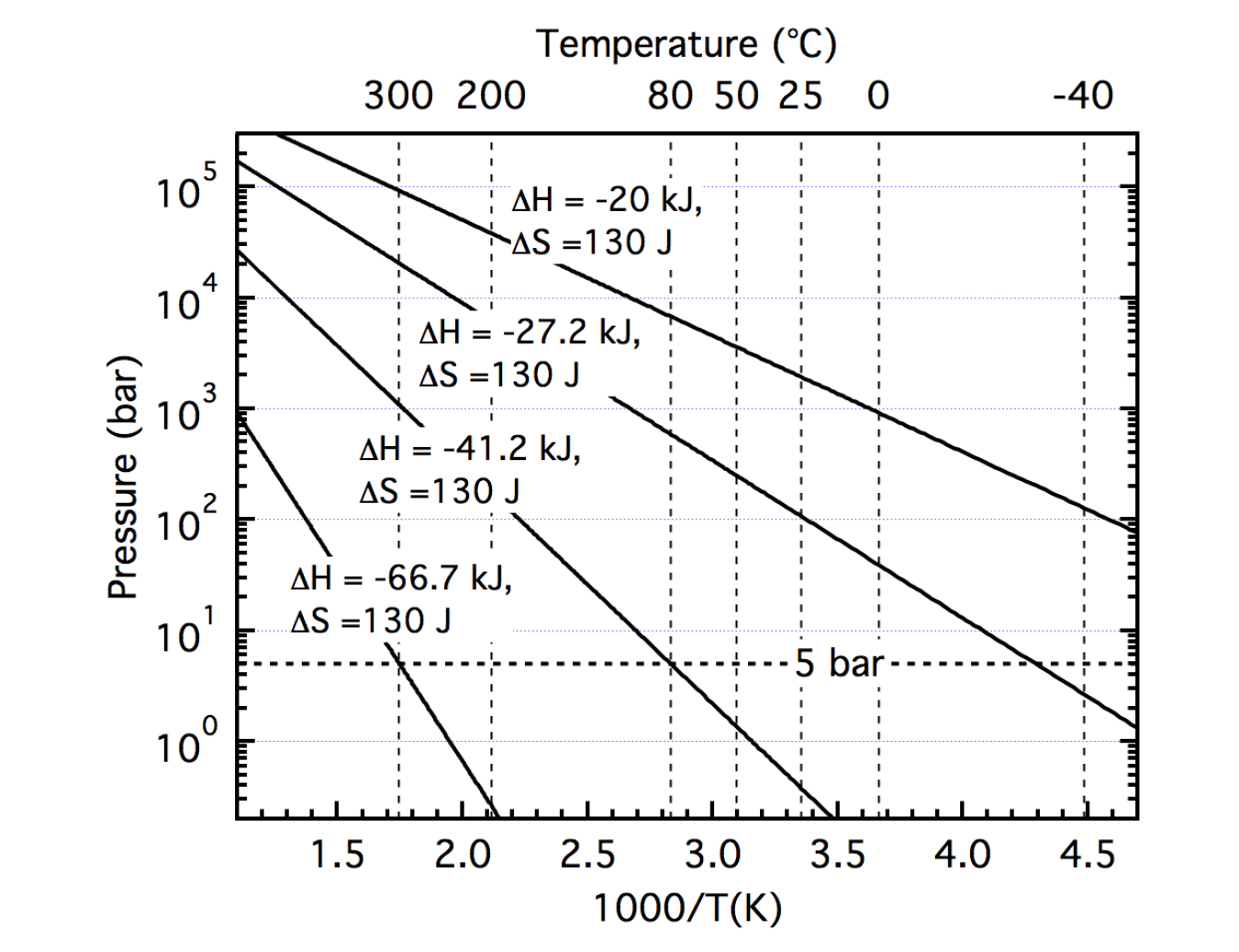
Hình 2. Các đường van't Hoff được tính toán minh họa phạm vi entanpy tạo ra áp suất cân bằng 5 bar giả sử entropy không đổi.
Cũng cần phải biết giá trị entropy vì độ dốc và entanpy ở một áp suất và nhiệt độ cụ thể có thể thay đổi tùy thuộc vào giá trị của ΔS. Mặc dù người ta thường cho rằng ΔS bị chi phối bởi sự thay đổi entropy của pha khí khi hydro biến đổi từ khí hai nguyên tử thành hydro nguyên tử thành mạng kim loại, ΔSH2, Rudman và Sandrock7 lưu ý rằng một sự thay đổi lớn về giá trị entropy của pha khí sẽ đi kèm với một thay đổi nhiệt độ. Tuy nhiên, nhận thức được giá trị gần như không đổi của ΔS được xác định từ nghiên cứu thực nghiệm, Oates và Flanagan8 lưu ý rằng đối với một áp suất ổn định nhất định, ΔS gần như không đổi sẽ được cho là do entropy hydrua có độ dốc tăng tương tự như được xác định từ mô hình dao động Einstein. Giả sử rằng sự thay đổi entropy ΔS gần như tương đương với sự thay đổi entropy của khí ở mức ~130 J/mol K, thì áp suất cân bằng 5 bar trong phạm vi nhiệt độ từ −40°C đến 80°C đòi hỏi entanpy trong khoảng từ 27 đến 41 kJ/ mol hydro (Hình 2).
Nghiên cứu vật liệu hydrua kim loại của HFTO gần đây tập trung vào cái gọi là hydrua phức thường bao gồm các nguyên tố kiềm hoặc kiềm thổ được liên kết ion với anion phức. Bản thân các anion có thể bao gồm các nguyên tử trung tâm thường là kim loại chuyển tiếp hoặc kim loại nhóm chính hoặc kim loại (ví dụ: Fe, Ni, B, Al) hoặc N, mà hydro được liên kết cộng hóa trị. Giống như hydrua kim loại, phản ứng giải hấp trong chuỗi hợp chất này có thể thu nhiệt khi giải phóng hydro. Với việc theo đuổi các vật liệu có mật độ trọng lượng và thể tích hydro cao hơn, việc sử dụng các hydrua phức tạp bao gồm các cation Z thấp mang lại khả năng sử dụng khi khử hydro hoàn toàn hydrua cân bằng hóa học.
Mức độ nỗ lực ngày càng tăng trong việc nghiên cứu loại vật liệu này có thể bắt nguồn từ công trình ban đầu của Bogdonovic9 khi ông phát hiện ra rằng quá trình khử hydro qua trung gian Ti có thể được thực hiện trong NaAlH4, trước khi tan chảy.10 Cũng như một số phản ứng khử hydro phức tạp, tuy nhiên, con đường phản ứng thực tế và cơ chế khuếch tán hiếm khi bao gồm một con đường đơn giản trong đó tất cả hydro liên kết được giải phóng trong phạm vi dung dịch rắn chỉ bao gồm các pha hydrua và không hydrua của các vật liệu này.11 Trong các hệ thống có đặc tính ion của liên kết của hiđrua phức tạp đóng vai trò tĩnh điện
các lực có thể chi phối và áp đặt các giới hạn lên các cơ chế khuếch tán có thể cần thiết để tác động đến độ linh động của nguyên tử cần thiết cho quá trình hydro hóa/khử hydro trong một tinh thể khối. Do đó, HFTO tập trung vào việc cải thiện không chỉ khả năng đo thể tích và trọng lượng mà còn cả động học hấp phụ và giải hấp hydro cũng như nhiệt động lực học phản ứng. Hiệu ứng đạp xe dài hạn cũng đang được nghiên cứu.
Người giới thiệu
Vetrano, J.B. "Hydrua làm vật liệu điều tiết neutron và phản xạ."Kỹ thuật và Thiết kế Hạt nhân (14:3), 1970; P. 390.
Trẻ, K-H.; Nei, J. "Hiện trạng phát triển hợp kim lưu trữ hydro cho các ứng dụng điện hóa."Tài liệu (6), 2013; trang 4574–4608.
Felderhoff, M.; Bogdanovic, B. "Hydrua kim loại nhiệt độ cao làm vật liệu lưu trữ nhiệt cho các ứng dụng năng lượng mặt trời và các ứng dụng liên quan."Tạp chí Quốc tế về Khoa học Phân tử (10:1), 2009; trang 325–344.
Lototskyy, M.V.; Yartys, V.A.; Pollet, B.G.; Bowman, R.C. Jr. "Máy nén hydro hyđrua kim loại: Đánh giá."Tạp chí Quốc tế về Năng lượng Hydro (39), 2010; trang 5815–5851.
Wang, Z.M.; Lý, V.; Chan, S.L.I. "Đánh giá màng/màng hợp kim để tách hoặc tinh chế hydro."Tạp chí Đất hiếm (23), 2005; trang 611–616.
Switendick, A.C. Trong Hydro trong kim loại I. Các chủ đề về Vật lý ứng dụng, Tập. 28. G. Alefeld và J. Völkl, biên tập. Berlin: Springer, 1978.
Rudman, P.S.; Sandrock, G.D. "Luyện kim Hyđrua có thể sạc lại."Tạp chí Khoa học Vật liệu Thường niên (12), 1982; trang 271–294.
Oates, WA; Flanagan, T.B. “Độ hòa tan của hydro trong kim loại chuyển tiếp và hợp kim của chúng.”Tiến bộ trong Hóa học chất rắn (13), 1981; trang 193–283.
Bogdanovic, B.; Schwickardi, M.J. "Hyđrua nhôm kim loại kiềm pha tạp Ti là vật liệu lưu trữ hydro có thể đảo ngược mới tiềm năng."Tạp chí Hợp kim và Hợp chất (253–254), 1997; trang 1–9.
Reilly, JJ; Wiswall, R.H.; Waide, C.H.Lưu trữ hydro cho phương tiện cơ giới bằng hydrua kim loại. Báo cáo của EPA TEC-75/001.
Callini, E.; Borgschulte, A.; Hugelshofer, C.L.; Ramirez-Cuesta, A.J.; Züttel, A. “Vai trò của Ti trong Alanates và Borohydrides: Xúc tác và trao đổi chất.”Tạp chí Hóa lý C (118), 2014; trang 77−84.
Mời các đối tác xem hoạt động của Công ty TNHH Pacific Group.
FanPage: https://www.facebook.com/Pacific-Group
YouTube: https://www.youtube.com/@PacificGroupCoLt






